Titik Beku
Titik
beku larutan adalah suhu pada saat tekanan uap cairan sama dengan tekanan uap
padatannya. Tekanan luar tidak terlalu berpengaruh pada titik beku. Pada postingan sebelumnya sudah dibahas bahwa pada tekanan 760 mmHg (1 atm), air membeku pada
suhu 0 °C, sedangkan pada tekanan 4,58 mmHg air akan membeku pada suhu 0,0099 °C.
Penurunan Titik Beku Larutan Nonelektrolit
Larutan
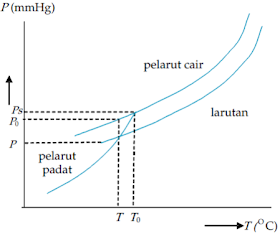
akan membeku pada suhu yang lebih rendah dari pelarutnya. Perhatikan gambar di bawah
ini!
Pada
setiap saat tekanan uap larutan selalu lebih rendah daripada pelarut murni. Ini
berarti penurunan tekanan uap jenuh menyebabkan penurunan titik beku larutan.
dengan
Tf
pelarut (Tf°) = titik beku pelarut (°C)
Tf
larutan (Tf ) = titik beku larutan (°C)
Hubungan
antara penurunan titik beku dengan molalitas larutan dirumuskan sebagai
berikut.
dengan
m =
molalitas larutan (molal)
Kf =
tetapan penurunan titik beku molal(°C/molal)
Beberapa
harga tetapan penurunan titik beku molal pelarut diberikan pada tabel berikut
ini.
Contoh Soal 1
Tentukan
titik beku larutan glukosa 9 gram glukosa dalam 300 gram air, Kf air
= 1,86 °C/molal.
Jawab:
Diketahui:
massa
glukosa = 9 gr
massa
air = 300 gr = 0,3 kg
Kf air
= 1,86 °C/molal.
Ditanyakan: Tf
= ?
Penyelesaian:
n
glukosa = massa/Mr
n
glukosa = 9 gr/(180 gr/mol)
n
glukosa = 0,05 mol
m = n/p
m = 0,05
mol/0,3 kg
m =
0,17 molal
ΔTf = m.Kf
ΔTf = 0,17 molal.1,86 °C/molal
ΔTf = 0,3162 °C
Titik
beku larutan = titik didih pelarut - Tf
Titik
beku larutan = 0 - 0,3162 °C
Titik
beku larutan = - 0,3162
°C
Jadi,
titik beku larutan tersebut adalah -0,3162 °C.



Bagaimana kalau soal nya terdapat nilai Ar dari unsur glukosa
BalasHapusYa mencari Mr seperti biasa, dijumlahkan Ar nya. Di contoh soal itu sudah diberi Mr nya, jadi gk perlu mencari dari Ar nya lagi.
Hapus